Legemidler og biotek
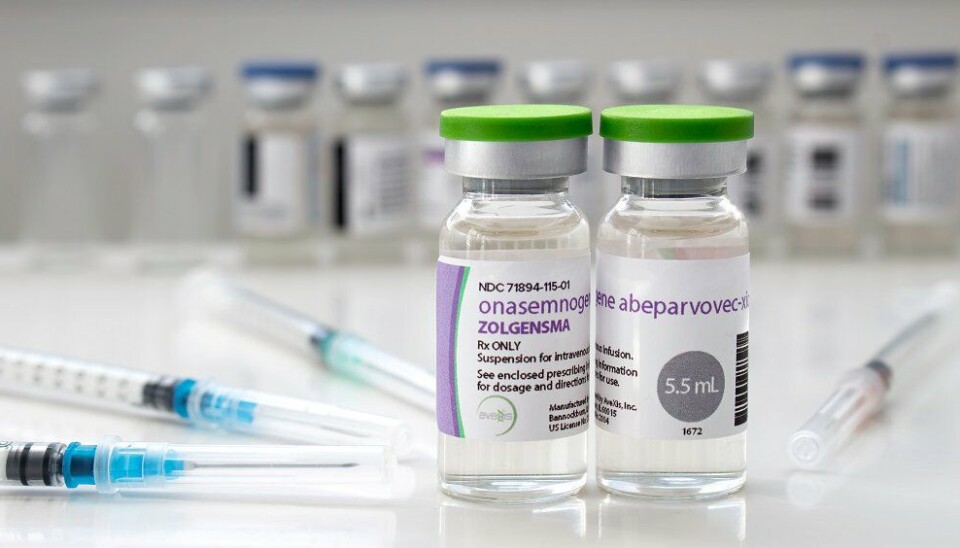
Beslutningsforum avgjør nå om verdens dyreste legemiddel skal tilbys norske spedbarn
Mandag faller avgjørelsen om genterapien Zolgensma skal innføres i pasientbehandlingen av spedbarn med den genetiske sykdommen spinal muskelatrofi. For første gang skal Beslutningsforum ta stilling til en resultatbasert avtale som innebærer at produsenten Novartis må tilbakebetale et betydelig beløp dersom barna som behandles med Zolgensma dør eller trenger permanent pustehjelp
I et forsøk på å dempe kostnadene ved avansert legemidler vedtok Beslutningsforum i mai at Sykehusinnkjøp kunne starte forhandlingene med Novartis Gene Therapies basert på en prismodell der sykehusene og Novartis deler den økonomiske risikoen basert på resultatet av behandlingen med Zolgensma.
Slike avtaler kalles resultatbaserte eller verdibaserte og har aldri tidligere vært brukt i innkjøp av legemidler i Norge. Zolgensma er en engangsbehandling som er designet for å ha livslang effekt. Om lag 7 pasienter diagnostiseres årlig med SMA i Norge og om lag fire til seks pasienter kan være aktuelle for behandling med Zolgensma.
Krever store prisreduksjoner
Prisen for Zolgensma ut av apotek uten rabatt er i følge Sykehusinnkjøp i overkant av 27 millioner kroner per pasient. En slik pris har Beslutningsforum sagt tydelig fra om er helt uaktuell å betale. På sitt møte i mai år ble det fattet følgende vedtak: “Beslutningsforum for nye metoder ber leverandøren redusere prisen på produktet vesentlig slik at det er mulig å oppfylle prioriteringskriteriene. Dette er en forutsetning for at arbeidet med alternativ [resultatbasert] avtale kan fortsette.”
Nå har Sykehusinnkjøp og Novartis ferdigforhandlet avtalen og på mandag skal de fire direktørene i de regionale helseforetakene som utgjør Beslutningsforum avgjøre om avtalen er god nok for staten. Avtalen er hemmelig, men vi er kjent med at den innebærer at Novartis gir en betydelig rabatt på engangsbehandlingen og skal tilbakebetale et betydelig beløp dersom genterapien ikke ikke virker helt eller delvis. Hva som er resultatmålet for behandlingen og endepunktet for når en eventuell tilbakebetaling skal skje og beløpets størrelse har vært sentrale punkter i forhandlingene.
Beslutningsforum for nye metoder har publisert en rekke interne saksdokumenter. Betydelige deler av innholdet er sladdet, men det fremgår at en tilbakebetaling vil inntre dersom barna som er behandlet med Zolgensma dør eller trenger permanent pustehjelp. I tillegg nevner de interne dokumentene et tredje kriterium, men dette er sensurert.
Stor prinsipiell betydning
Vedtaket som på mandag skal gjøres i Beslutningsforum er av stor prinsipiell betydning og følges med argusøyne av legemiddelindustrien, pasientenes pårørende og legene.
Det er nemlig forventet at et 10-talls gen-, celle- eller vevsterapier - som med en felles betegnelse kalles avanserte legemidler (Advanced Therapy Medicinal Products) - vil komme opp til behandling i Beslutningsforum innen relativt kort tid. De avanserte legemidlene utfordrer det etablerte systemet for refusjon av legemidler på flere måter. For det første er prisen for disse engangsbehandlingene langt høyere enn for gjentagende behandling. I tillegg er det usikkerhet rundt langtidseffekten. Det har medført at Beslutningsforum så langt bare har innført to avanserte legemidler. Det er celleterapien/CAR-T behandlingen Kymriah til behandling av akutt lymfoblastisk leukemi (ALL) for barn og unge og genterapien Luxturna til behandling av synstap på grunn av arvelig retinal dystrofi som skyldes mutasjoner i RPE65-genet.
Ved å inngå resultatbaserte avtaler kan legemiddelprodusentene og sykehusene samle mer såkalt “real world-evidence” som viser hvordan avanserte behandlinger faktisk fungerer. Og avtalen for Zolgensma kan bidra til å sette scenen for avtalene som skal inngås på de kommende avanserte legemidlene.
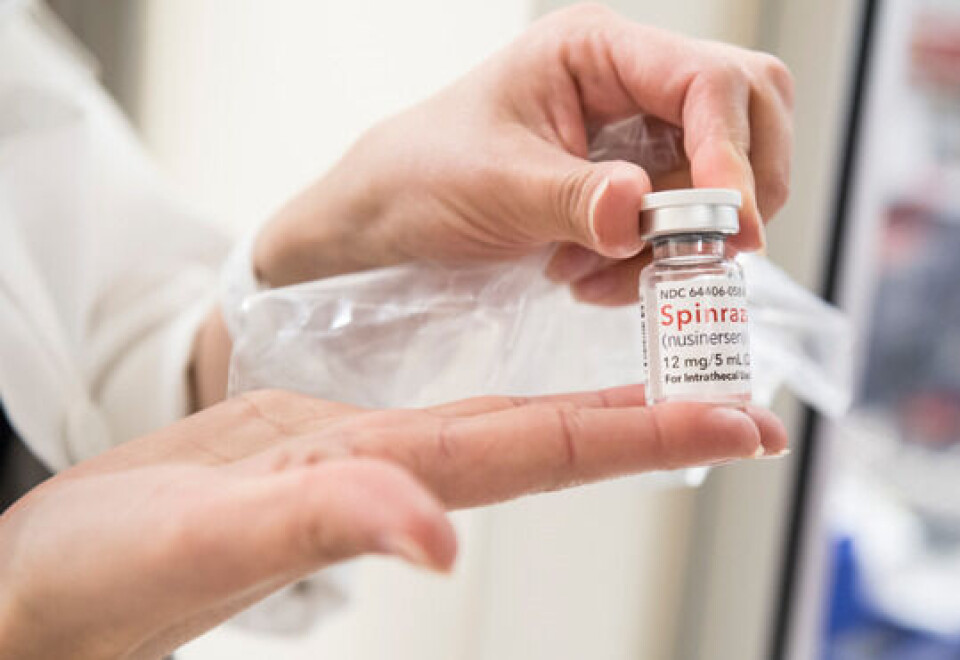
Et nøkkelspørsmål: Er Zolgensma dyrere enn Spinraza
Et nøkkelspørsmål i Beslutningsforums diskusjoner på mandag vil dreie seg om kostnadene ved å innføre Zolgensma er høyere enn den etablerte behandlingen med Spinraza (nusinersen).
I februar 2018 godkjente Beslutningsforum å ta i bruk Spinraza ved SMA på gitte vilkår som i praksis er tilfredsstilt hos de fleste barn med nydiagnostisert SMA. Også denne behandlingen er svært kostbar - men har god dokumentert effekt. Norge bruker dermed allerede i dag mange millioner kroner årlig på behandling med Spinraza som administreres med en sprøyte i ryggraden (intratekalt) hver fjerde måned. Noen pasienter må legges inn på sykehus for å motta legemiddelet, og noen pasienter må sederes.
Mens Zolgensma er en engangsbehandling må Spinraza gis livslangt. Barn med SMA trenger syv sprøyter Spinraza det første året, og deretter tre sprøyter årlig med medisinen resten av livet. I følge det svenske legemiddelverket (TLV) er maksimalprisen prisen på Spinraza om lag 80 000 per behandling. Prisen blir dermed 4,8 millioner kroner det første året og deretter om lag 2,4 millioner kroner årlig. Den svenske prisen er trolig ikke langt unna prisen for legemidlet i Norge. Det er dessuten lavere administrasjons- og oppfølgingskostnader for Zolgensma enn for Spinraza. Det betyr at kostnadene per pasient for de to behandlingene utlignes etter noen år - da vil Zolgensma «gå i null» i forhold til Spinraza.
Det danske Medicinrådet - som tilsvarer Beslutningsforum - vedtok den 26. mai i år å innføre Zolgensma som standardbehandling i Danmark. Medicinrådet estimerer at det tar mellom 8-15 år før kostnadene per pasient for de to behandlingene utlignes, men understreker at det er betydelig usikkerhet. Statens legemiddelverk har utført en kostnadsanalyse basert på maksimalprisene der kostnadsforskjellen mellom behandling med Zolgensma og Spinraza blir null etter om lag 9 år.
Sverige mener Zolgensma er kostnadseffektiv
Det svenske legemiddelverket - TLV- konkluderer i en helseøkonomisk analyse at Genterapien Zolgensma er kostnadseffektiv i behandlingen av den alvorligste formen for sykdommen spinal muskelatrofi (SMA). Når Zolgensma brukes mot den mest alvorlige formen for SMA - type 1 - og sammenliknes med dagens standardbehandling Spinraza (nusinersen), viser TLV sin helseøkonomiske analyse at merkostnaden per vunnet kvalitetsjustert leveår (QALY) for Zolgensma er mellom 850 000 og 3,2 millioner svenske kroner.
Det store kostnadsspriket skyldes ulike forutsetninger som TLV har gjort for hvor lenge engangsbehandlingen virker. Den laveste kostnaden per kvalitetsjustert leveår (850 000) forutsetter at behandlingen varer livet ut, mens kostnaden på 3,2 millioner forutsetter at behandlingen bare virker i 10 år. Med en antagelse om en langtidseffekt på 15 år , vil prisen per QALY være 1,7 millioner kroner i følge TLVs beregning.
I Sverige har TLV en rettesnor som tilsier at en pris på 2 millioner svenske kroner per vunnet kvalitetsjustert leveår kan betraktes som kostnadseffektiv hvis det er tale om alvorlige, sjeldne sykdommer. Dermed ville Novartis sin tilbudte pris for Zolgensma på 20 726 870 svenske kroner havne innenfor grensen som svenske myndigheter er villig til å dekke.
Nå er det opp til NT-rådet (Rådet för Nya Terapier) å ta en beslutning om legemidlet skal innføres eller ikke. NT-rådet tilsvarer det norske Beslutningsforum.