Legemidler og biotek
Banebrytende CAR-T studie med T-celler fra friske donorer
På årsmøtet til i American Society of Hematology er det presentert flere banebrytende kliniske studier med CAR-T celleterapi innen en rekke blodkreftdiagnoser. - En av de store nyhetene var en tidligfasestudie der man behandler myelomatosepasienter med T-celler fra friske donorer. Denne teknologien har potensiale til å revolusjonere CAR-T behandlingen, sier overlege Fredrik Schjesvold på Oslo Myelomatosesenter.
Teknologien kalles allogen CAR-T og er genmodifiserte T-celler fra friske donorer. Disse cellene er ikke tilpasset hver enkelt pasient men er såkalt “off the shelf” eller hyllevare på godt norsk, hvor alle pasientene i studien får de samme aktiverte T-cellene.
Det er Biotekselskapet Allogene som har utviklet den nye CAR-T teknologien og på mandag presenterte de fase 1 studien ALLO-715.
Responsraten på relativt små doser er på 60 prosent, sier Fredrik Schjesvold.
Modifiserer T-celler med genteknologi
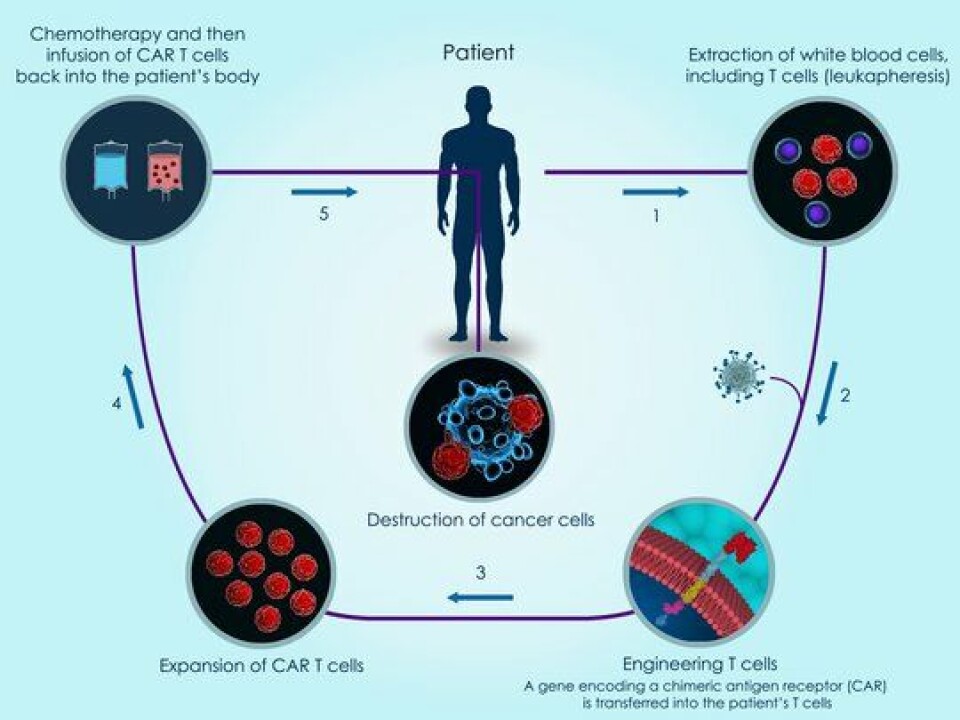
CAR-T er en form for immunterapi. Ved å modifisere immunceller til å angripe kreftcellene kan man instruere immunsystemet til å angripe kreftcellene med stor grad av spesifisitet. Denne behandlingen har radikalt bedret prognosen for flere typer blodkreft.
Tradisjonelt har CAR-T celleterapi gått ut på å hente ut immunceller, T-celler, fra pasientens eget blod. Allogenes teknologi gjør det nå mulig å ta i bruk T-celler fra friske donorer. Disse T-cellene blir så genteknologisk endret. Et nytt gen blir satt inn i T-cellene slik at disse blir i stand til å gjenkjenne og drepe kreftcellene. Deretter settes de inn i pasienten. Til slutt sprøytes millioner av slike immunceller tilbake i kroppen til pasienten som så angriper kreftcellene.
Høster T-celler fra frisk donorer
Konkurrentene til Allogene er Janssen med sin cilta-cel og Bristol Myers Squibb med sin ide-cel. Disse to selskapene høster T-celler fra den enkelte pasient og produserer dermed CAR-T behandling individuelt for hver pasient - det vil si autologt. Dette er en kostbar og ikke minst tidkrevende prosess, men arbeidet med "hylleprodukter" er altså i gang.
Allogene sin CAR-T teknologi heter ALLO-715 og i likhet med cilta-cel ide-cel gjenkjenner ALLO-715 et protein som heter BCMA (B-celle-modningsantigen) som finnes på myelomatosecellene.
Ikke like effektiv
Studien viser at det er mulig å produsere allogene T-celler og trygt administrere disse. Effekten - selv om den er lavere enn det de autologe rivalene kan vise til - er likevel et godt startpunkt som kan bedres når Allogene går videre med dose-eskaleringstudien og senere inn i effektstudiene.
Allogene sin CAR-T teknologi har dessuten fordeler som gjør at den kan være konkurransedyktig selv om denne BCMA-behandlingen altså ikke er like effektiv som cilta-cel og ide-cel. Median tid fra pasientene ble innrullert i studien var fire dager, og det er noe som de autologe celleterapiene ikke kan matche.
Enklere og billigere
Fredrik Schjesvold leder en CAR-T studie med ide-cel og forteller det kan ta opp til tre måneder fra man starter å høste pasientens blod til selve behandlingen starter.
- I løpet av denne tiden vil sykdommen forverre seg, og pasientene kan i verste fall bli så syke at de ikke lenger er aktuelle for CAR-T behandlingen. Dersom videre studier viser at allogen CAR-T behandling er trygt og effektivt vil dette kunne revolusjonere CAR-T behandlingen siden det vil gjøre det mye enklere, mindre tidkrevende og billigere å behandle pasientene. Dermed kan potensielt flere pasienter få tilgang til CAR-T behandling, sier han. - Ved allogen teknologi benyttes friske T-celler fra en donor, mens ved autolog CAR-T behandling høster vi T-celler fra en pasient som har har hatt myelomatose i mange år og har blitt behandlet med en rekke legemidler. Det er åpenbart at disse T-cellene ikke nødvendigvis er like gode som de som høstes fra friske pasienter, sier Schjesvold.
- Når er det realistisk at behandling med allogen CAR-T kan innføres?
- Dette er første gang vi ser data som viser at denne teknologien virker i klinikken. Dataene er lovende, men vi må se lengre tidsserier før vi kan konkludere. Foreløpig er denne teknologien eksperimentell, så det er mer et spørsmål om den kommer enn når den kommer, sier Schjesvold.
Dette er de autologe CAR-T behandlingene innen myelomatose
Janssen har presentert nye data fra CARTITUDE-1 studien på #ASH20 der myelomatosepasientene fikk én infusjon av cilta-cel. 97 prosent av pasientene oppnådde respons av behandlingen og 67 prosent oppnådde komplett respons (CR) hvilket betyr at de ikke hadde noe tegn til kreftceller i benmargen. Studien inkluderte 97 pasienter med avansert myelomatose. Deltakerne var veldig syke, og kreften hadde utviklet seg etter at de tidligere var behandlet med en median på seks ulike behandlinger.
Bristol Myers Squibb er med sin ide-cel fremst i CAR-T løypa. I likhet med cilta-cel og Allo 715 gjenkjenner ide-cel et protein som heter BCMA (B-celle-modningsantigen) som finnes på myelomatosecellene. Ide-cel har ennå ikke markedsføringstillatelse hverken i USA eller Europa. Fredrik Schjesvold sier at han forventer at ide-cel vil få godkjenning i Europa i januar 2021. En godkjenning av ide-cel vil være et stort gjennombrudd fordi den da vil oppfylle et stort udekket medisinsk behov og demonstrere at CARs også kan binde seg til andre målcellers overflate enn CD19 - i dette tilfellet CARs som er laget for å gjenkjenne BCMA som uttrykkes på myelomatoseceller.
Legemiddelverket gjennomfører nå en hurtig metodevurdering med grunnlag i søkt indikasjon fra Bristol Myers Squibb som er: “Behandling av myelomatose hos voksne pasienter som har fått minst tre tidligere behandlinger, inkludert proteasomhemmer, immunmodulatorisk middel og et anti-CD38 monoklonalt antistoff.”
I sin studie som ligger til grunn for søknaden om godkjenning i USA og Europa oppnådde man en en responsrate på 82 prosent og en komplett respons på 39 prosent. Median progresjonsfri overlevelse var 12,1 måneder. 6 prosent av ide-cel pasientene opplevde moderat til alvorlig CSS der en pasient døde.
Dette er virkemekanismen til Ide-cel
Produktet er en CAR T-celleterapi der blod er tatt fra pasienten. Leukocytter er isolert ved bruk av en blodcelleseparator (leukocyttafarese) og sendt til et produksjonssenter. Cellene får deretter satt inn, ved hjelp av et såkalt vektorvirus, et gen som koder for en kimerisk antigenreseptor (CAR) som er laget for å gjenkjenne BCMA (B-celle-modningsantigen) som utrykkes på myelomatoseceller. Vektorvirusets DNA inkorporeres i cellens DNA slik at cellene uttrykker CAR reseptoren på cellens overflate. CAR har både antigen bindende og T-celleaktiverende funksjoner. CAR-T-cellene blir sendt tilbake til sykehuset der de blir tilbakeført til pasienten. Når disse CAR-T-cellene binder BCMA på målcellene, blir målcellene destruert ved bruk av ordinære mekanismer til cytotoksiske T-celler.