Legemidler og biotek, Helseteknologi
Nyfødtscreening av spinal muskelatrofi har kjørt seg fast i helsebyråkratiet
I over ett år har foreldre og fagmiljøet ventet på at helsemyndighetene skal inkludere den arvelige sykdommen spinal muskelatrofi (SMA) i nyfødtscreeningen. Men til tross for at helseminister Bent Høie har lovet fortgang i saksbehandlingen, har saken kjørt seg fast i helsebyråkratiet. SMA er en av de vanligste årsakene til tidlig barnedød i Norge.
I Norge blir det født rundt 60 000 barn årlig. I sjeldne tilfeller kan barnet ha en medfødt sykdom, selv om det virker helt friskt fra fødselen. Alle nyfødte i Norge får derfor tilbud om nyfødtscreening, hvor man undersøker barnets blod for 25 alvorlige medfødte sykdommer. Men foreløpig testes det ikke for SMA - som er en av de vanligste årsakene til tidlig barnedød i Norge - og som det siden 2018 har eksistert en effektiv behandling for.
Kan leve et tilnærmet normalt liv
De 25 sykdommene som screenes for er sjeldne, men hvert år er det mellom 50 og 60 barn som fanges opp ved hjelp av nyfødtscreening. For disse er det av stor betydning at de har blitt funnet kort tid etter fødsel slik kan man starte behandling før symptomene oppstår. Disse barna må bli oppdaget raskt for at de skal få behandling så tidlig som mulig, og på den måten unngå irreversible skader og i verste fall død. De kan da få god behandling tidlig, ofte før barnet i det hele tatt har hatt symptomer. Flesteparten av barna kan da leve tilnærmet normale liv.
Nyfødtscreeningens fulle navn er “Nasjonal behandlingstjeneste for screening av nyfødte og avansert laboratoriediagnostikk ved medfødte stoffskiftesykdommer”, og er organisatorisk forankret i Barne- og ungdomsklinikken på Oslo Universitetssykehus (OUS). Hver dag mottar Nyfødtscreeningen om lag 250 prøver fra de 49 fødestedene rundt om i Norge.
Enkel blodprøve avdekker arvelig sykdom
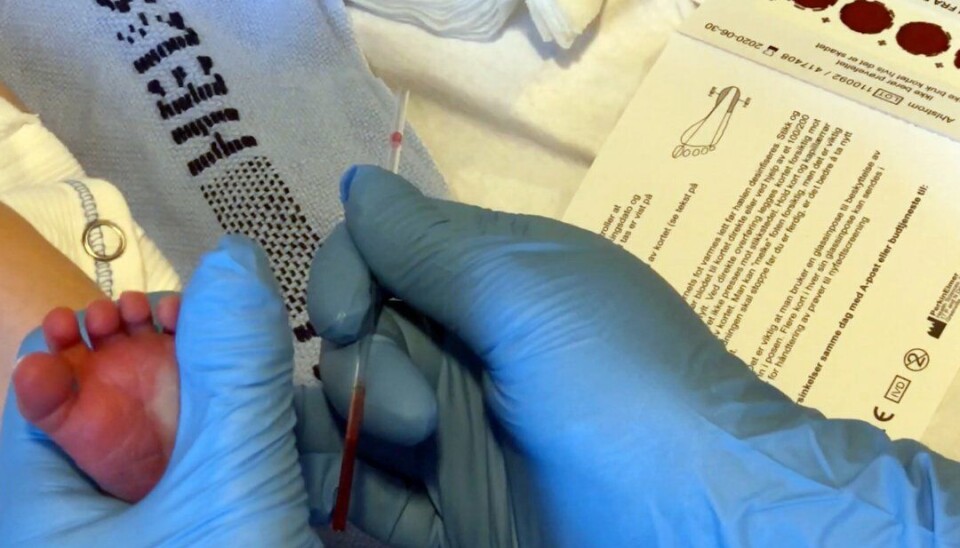
Når et barn blir født tas det en blodprøve i hælen omtrent to døgn etter fødsel. Denne kan avdekke 25 sjeldne sykdommer. Men nå ønsker altså fagmiljøet å utvide tilbudet til å gjelde 26 slike sykdommer.
Siden 16. desember 2019 har Nyfødtscreeningen og OUS søkt om å få screene for den alvorlige sykdommen spinal muskelatrofi (SMA), hvor nye legemidler har revolusjonert behandlingen av sykdommen. Da vil man kunne avdekke sykdommen i løpet av den aller første leveuken.
Men Helsedirektoratet sendte søknaden i retur fordi de vurderte at de trengte mer informasjon for å gjøre en helhetlig vurdering. Nå må søknaden gjennom flere byråkratiske prosesser før regjeringen ved helse- og omsorgsministeren endelig vil vedta om test for SMA skal inngå i nyfødtscreeningen. Initiativet fra Nyfødtscreeningen og OUS har blitt sendt ut på en lang reise i helsebyråkratiet, og saken er fremdeles langt unna en eventuelt positiv beslutning.
Nå mener fagmiljøet at det haster med å få en beslutning som inkluderer SMA i nyfødtscreeningprogrammet, slik at sykdommen kan oppdages så tidlig som mulig etter fødsel.
I denne videoen kan du hvordan spedbarn testes for genetiske sykdommer.
- Det er viktig å teste for SMA siden behandlingen er mer effektiv jo tidligere barna identifiseres. Klinisk diagnostikk, det vil si etter sykdomsdebut, medfører forsinket identifisering av aktuelle barn og forsinket behandling, forteller Janne Strand. Hun er spesialingeniør på Avdeling for nyfødtscreening og har ansvaret for de genetiske testene. Hun og resten av fagmiljøet mener det tar for lang tid å få innført SMA i nyfødtscreeningen. Men mer om viktigheten av tidlig diagnostisering og behandling litt senere i denne artikkelen.
Helseministeren har det siste ordet
Det tok over et halvt år bare å få slått fast saksbehandlingsprosedyren for hvordan SMA eventuelt skal innføres i nyfødtscreeningen.
Det drøye halvåret ble brukt til å slå fast at nyfødtscreeningprogrammet er særskilt regulert gjennom bioteknologiloven ogforskrift om genetisk masseundersøkelse av nyfødte. Hvilke sykdommer nyfødte screenes for er altså regulert gjennom forskrift, og Helsedepartementet slår den 12. juni 2020 endelig fast at en eventuell utvidelse av testtilbudet bare kan gjøres etter en forskriftsendring. Det betyr at en beslutning om utvidelse av nyfødtscreeningprogrammet til å omfatte testing for SMA bare kan tas av regjeringen - i praksis av helse- og omsorgsminister Bent Høie.
Statssekretær Anne Grethe Erlandsen sier dette i en e-post til HealthTalk:
-Jeg er klar over at Helsedirektoratet rett før jul mottok en søknad fra Helse Sør-Øst om utvidelse av nyfødtscreeningprogrammet. Vi vil ta en avgjørelse når vi har mottatt vurderingen fra Helsedirektoratet.
Med denne kunnskapen sender Helsedirektoratet den 23. juni et brev til Nyfødtscreeningen der de informerer om at følgende prosess skal følges ved endring av nyfødtscreeningprogrammet:
- Helse Sør-Øst RHF ved Nyfødtscreeningen, utarbeider søknad om utvidelse av nyfødtscreeningprogrammet.
- Søknaden skal utarbeides i tråd med kriterier for nasjonale screeningsprogrammer og i samråd med tjenestens faglige referansegruppe, og oversendes Helsedirektoratet for vurdering. Søknaden skal omfatte forslag til ny beskrivelse av tjenestens innhold.
- Helsedirektoratet vurderer søknaden og innhenter om nødvendig ytterligere informasjon/kunnskapsgrunnlag, inkludert etiske vurderinger, helseøkonomiske og/eller kostnadsberegninger. Ved behov for oppdatert kunnskapsoppsummering eller metodevurdering utarbeider Folkehelseinstituttet dette etter bestilling fra Helsedirektoratet. Ved behov innhentes også ytterligere innspill og råd fra de regionale helseforetakene og fagmiljø.
Søknaden vurderes etter regelverket for nasjonale tjenester, bioteknologiloven og forskrift for masseundersøkelser av nyfødte. I tillegg gjøres en helhetsvurdering av søknaden opp mot screeningkriteriene, prioriteringskriteriene, etiske implikasjoner og andre konsekvenser av endringen, inkludert økonomiske konsekvenser.
- Helsedirektoratet oversender en anbefaling til Helse- og omsorgsdepartementet
- Helse- og omsorgsdepartementet sender forslag om endring av Forskrift om masseundersøkelser av nyfødte på høring
- Etter høring beslutter HOD eventuell endring av forskrift, og Helsedirektoratet gir beskjed til Helse Sør-Øst RHF om at søknaden er godkjent og at endringen implementeres i Nyfødtscreeningen.
Den 2. november 2020 sendte Helse Sør-Øst en komplett søknad om utvidelse nyfødtscreeningprogrammet til Helsedirektoratet. Her ligger saken nå til vurdering og skal gjennom en omfattende saksbehandling. Helsedirektoratet skal blant annet vurdere om det er behov for at Folkehelseinstituttet gjennomfører en metodevurdering. En slik vurdering vil i så fall ta minimum et halvt år.
I september i fjor sier helseministeren til TV2 at det er en stor beslutning som skal tas men at han vil gjøre det han kan for at prosessen blir så kort som mulig.
– Så snart søknaden har kommet, vil jeg se på muligheten for å gjøre noen parallelle løp, slik at man korter ned tiden, sa han til TV2. Nå er søknaden under behandling hos Helsedirektoratet, men det er uklart om Høie har gjort noen tiltak som kan korte ned saksbehandlingen.
Her kan du se en oversikt over saksbehandlingen som er gjort og den som gjenstår for om SMA eventuelt blir innført i Nyfødtscreeningen.
Omfattende saksbehandling
Divisjonsdirektør Johan Torgersen i Helsedirektoratet bekrefter til HealthTalk at direktoratet har mottatt søknaden fra Helse Sør-Øst og at de har påbegynt arbeidet. - Vi vil vurdere om det skal innhentes ytterligere informasjon, sier han.
- Dere beskriver en omfattende prosess for videre søknadsbehandling. Når forventer du at Helsedirektoratet vil sende saken over til Helse- og omsorgsdepartementet?
- Direktoratet tar sikte på å ferdigstille saken så raskt som mulig, sier Torgersen.
- Dersom dere gir en anbefaling om innføring og departementet sender saken om forskriftsendring ut på høring - hvor lang høringsfrist er det ifølge Forvaltningsloven?
- Forvaltningsloven § 37 omhandler at berørte parter skal ha anledning til å uttale seg før forslag om forskriftsendringer blir utferdiget, endret eller opphevet. Det står ikke i lovteksten hvor lang høringsfrist saker skal ha. Normalt vil en høringssak ha mellom 6 uker og 3 måneders høringsfrist, så dette kan variere fra sak til sak.
- Når kan en forskriftsendring tidligst kunne bli vedtatt av regjeringen?
- Siden saken ikke er behandlet ferdig i direktoratet enda, og den skal behandles i departementet etter at vi har oversendt vår anbefaling, kan vi ikke si noe mer om tidsaspektet forteller Torgersen.
- Vi går med en vond følelse i magen
Spesialingeniør Janne Strand på Avdeling for nyfødtscreening mener det tar for lang tid å få innført SMA i nyfødtscreeningen.
- Vi har et håp om at dette skjer før sommeren. Vi som jobber på Nyfødtscreeningen og de som behandler disse barna går nå med en vond følelse i magen. Det fødes jo om lag 7 barn årlig som vil ha enorm nytte av en slik test. Å vente lengre får store konsekvenser for mange. Det er en vondt å gå å kjenne på, sier hun.
Spinal muskelatrofi er en alvorlig, arvelig sykdom som fører til tap av nerveceller i musklene, som igjen medfører muskelsvekkelse. Hvert år blir det født cirka 7 barn med SMA i Norge. Sykdommen kan ha ulik alvorlighetsgrad, og den mest alvorlige formen har vært en av de vanligste årsakene til tidlig barnedød i Norge. De mindre alvorlige formene gir tap av muskelkraft, og barna vil ikke kunne gå uten hjelp.
Det finnes en tilfredsstillende test som kan avsløre sykdommen med høy spesifisitet og sensitivitet slik at det blir en lav falsk positiv og falsk negativ rate. Det finnes også behandling som gir bedre effekt i tidlig stadium enn ved klinisk diagnostikk.
Men på avdelingen for nyfødtscreening på Rikshospitalet i Oslo mener fagpersonene at det tar for lang tid å få inn spinal muskelatrofi i screeningprogrammet.
Krever lite ekstra ressurser
- Det tas en blodprøve fra den nyfødtes hæl to døgn etter fødsel, og vi analyserer blodprøvene i løpet av samme dag. Vi bruker et arsenal av forskjellige metoder og teknologier for å finne de ca. 60 barna i året som har en av de 25 sykdommene i screeningprogrammet, forteller Janne Strand.
Gjennomføringen av SMA-testene krever lite ekstra ressurser. - For å screene for SMA trenger vi ikke mer blod eller ny teknologi og vårt laboratorium har alt nødvendig utstyr. Testen kan dessuten gjøres på samme måte som vi screener for alvorlig immunsvikt - SCID - i dag. Vi har også metode for å kunne si noe om alvorlighetsgraden av sykdommen, sier hun.
- Å jobbe med å hindre alvorlig sykdom og død hos barn er noe av det mest givende vi kan tenke oss. Og vi ønsker å gjøre mer. Nyfødtscreening er ikke aktuelt for sykdommer det ikke finnes behandling for, men medisinsk kunnskap og teknologi er i stadig utvikling, og nye behandlingsformer kommer på markedet årlig. For SMA finnes det effektiv behandling, sier hun.
Viktig å diagnostisere SMA før symptomene oppstår
Funn av SMA medfører imidlertid behov for svært kostbar behandling.
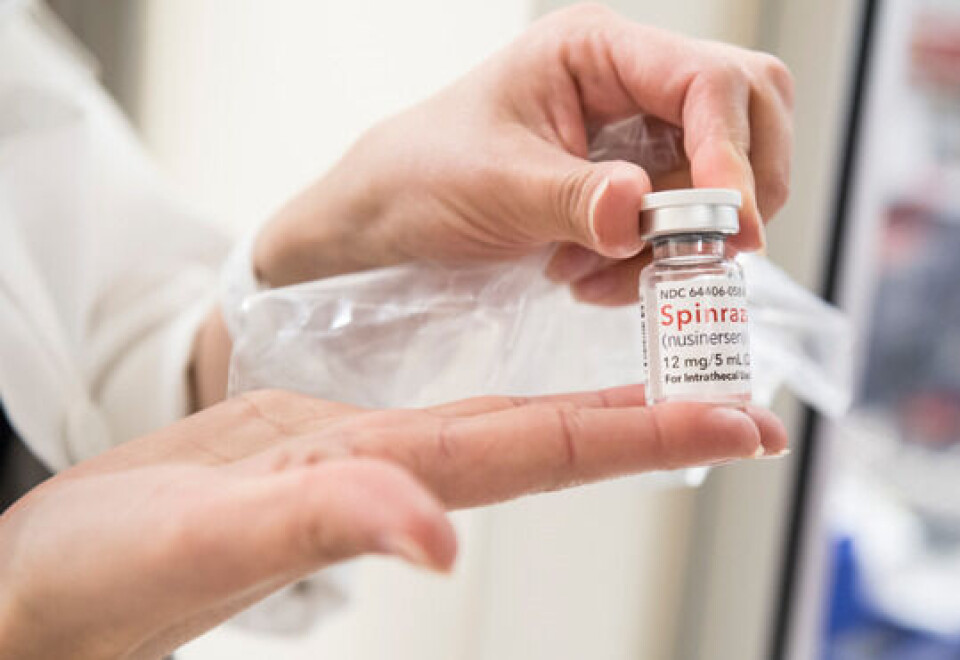
I februar 2018 godkjente Beslutningsforum å ta i bruk Spinraza (nusinersen) ved SMA på gitte vilkår som i praksis er tilfredsstilt hos de fleste barn med nydiagnostisert SMA. Behandlingen er svært kostbar men har god dokumentert effekt i litteratur. Norge bruker dermed allerede i dag mange millioner kroner årlig på behandling med Spinraza.
Barn og unge som har en SMA-diagnose, og barn som er født med SMA siden 2018 blir behandlet med dette legemidlet, men allerede tapte nerveceller kan ikke erstattes. Ved å oppdage sykdommen ved nyfødtscreening før symptomene oppstår, vil barn med SMA få enda bedre behandlingseffekt.
- Egentlig vil alle SMA barnepasienter som er aktuelle for Spinraza-behandling allerede i dag få et tilbud om dette etter at de har fått diagnosen stilt, men da med en viss diagnostisk forsinkelse. Hvis barna imidlertid får behandlingen tidligere er det bedre prognose, mindre grad av funksjonshemming og det vil også være samfunnsøkonomisk gunstig, sier Janne Strand.
- Dersom vi får lov til å teste for SMA vil barna i løpet av sine 1-2 første leveuker få stilt en SMA-diagnose og få igangsatt behandling med Spinraza på Rikshospitalet. Med dagens metode må det oppstå mistanke om at barnet er sykt og det kan ta måneder - for mange av barna kan virke friske ved fødselen. Det kan derfor ta flere måneder å få stilt en diagnose og igangsatt behandling, sier hun.
Viktig å starte behandlingen tidlig
All internasjonal og nasjonale erfaring tilsier at jo tidligere behandlingen kommer i gang jo bedre er effekten av behandlingen og prognosen. SMA skyldes tap av motornevroner grunnet mangel på SMN overlevelseproteinet, og behandlingens mål er å hindre nettopp dette. Tidlig økning av overlevelsesproteinet reduserer nevrontap.
Behandlingen med Spinraza øker mengden av proteinet som hindrer nervecelledød, og pasienten unngår dermed tap av muskelkraft. Det er godt dokumentert at jo tidligere behandlingen startes, jo mindre nervecelledød og desto bedre prognose for barnet. Det tar ofte flere måneder og år etter fødsel før sykdommen blir oppdaget. Denne tiden er kritisk for barna, fordi de mister flere motoriske nerveceller for hver dag de ikke får behandling.
Flere behandlinger er på vei
- Det er viktig å få en rask saksbehandling av å innføre nye genetiske tester i Nyfødtscreeningen. Nye analysemetoder og behandlinger er på vei og jeg vil anta at vi om ikke lenge også vil søke om å teste for sigdecelleanemi, andre typer immunsvikt på b-celler, sier Janne Strand, og hun viser til at det i USA testes for 64 medfødte sykdommer.
Nå er det også på vei nye effektive behandlinger for SMA. Den amerikanske legemiddelmyndigheten (FDA) godkjente engangsbehandlingen Zolgensma i mai 2019. Grunnlaget for godkjenningen var den innledende studien publisert i The New England Journal of Medicine som viste svært lovende effekter. Resultatene opprettholdes i oppfølgingsstudier.
CHMP som er Det europeiske legemiddelverket (EMA) sitt ekspertpanel for godkjenning av legemidler, ga i mai 2020 en betinget godkjenning av Zolgensma for visse pasienter: De med type 1 SMA (den alvorligste formen for sykdommen hvor den høyeste motoriske funksjon er liggende) og SMA-pasienter med opptil tre kopier av SMN2-genet.
Sa nei til å starte en hurtig metodevurdering
For behandlingen med genterapien Zolgensma ser det ut til å være enda viktigere med tidlig diagnose enn for Spinraza. Men et et vedtak i Bestillerforum setter bremsene på for en innføring av genterapien Zolgensma.
Den 26. oktober i fjor sa sa nemlig Bestillerforum nei til å starte en hurtig metodevurdering av Zolgensma til behandling av spedbarn med spinal muskelatrofi. Begrunnelsen var at Novartis ikke leverte tilstrekkelig dokumentasjon til at Statens legemiddelverk kan utarbeide en kostnad-nytte-vurdering. Dette betyr at en innføring av genterapibehandlingen er utsatt på ubestemt tid.
EU holder i disse dager på å vurdere et tredje SMA-legemiddel. Det er risdiplam fra Roche. Medisinsk direktør Karsten Bruins Slot i Roche Norge sier at de forventer at risdiplam blir godkjent i EU tidlig neste år. Det vil i så fall bety at risdiplam kan komme opp til vedtak i Beslutningsforum før sommeren 2021.
Risdiplam er studert i et bredt klinisk utviklingsprogram i SMA, med pasienter fra fødsel til 60-års alder og inkluderer også pasienter som tidligere er behandlet med andre SMA-behandlinger. Studiepopulasjonen representerer et bredt spekter av mennesker som lever med sykdommen. Risdiplam studeres i totalt fire studier. Det er studiene FIREFISH (SMA type 1) og SUNFISH (SMA type 2 og 3) som danner grunnlaget for søknaden om markedsføringstillatelse. I tillegg studeres risdiplam i studiene JEWELFISH (pasienter som tidligere har mottatt annen behandling) og RAINBOWFISH (nyfødte barn med genetisk påvist risiko for SMA, uten symptomer).
Risdiplam administreres oralt (gjennom munnen eller i ernæringssonde) som en flytende væske. Risdiplam er designet for å gi en vedvarende økning samt å bevare SMN-proteinnivået i sentralnervesystemet og i perifere vev. Risdiplam har en virkningsmekanisme som gjør at SMN2-genet hjelpes til å produsere mer funksjonelt SMN-protein i hele kroppen.