Legemidler og biotek
Beslutningsforum sier ja til å gi verdens dyreste legemiddel resultatbasert pris
I dag vedtok Beslutningsforum at Sykehusinnkjøp skal få lov til å inngå en prisavtale i innkjøpet av genterapien Zolgensma som aldri tidligere vært brukt i Norge. Frem til i dag har Beslutningsforum og sykehusinnkjøp kun vært villig til å inngå prisavtaler der legemiddelfirmaene gir prosentvise rabatter på legemidlenes listepris.
Det forteller Inger Cathrine Bryne til HealthTalk. Hun er administrerende direktør i Helse Vest RHF og ledet i dag sitt første møte i Beslutningsforum. Zolgensma brukes i behandling av barn med spinal muskelatrofi - SMA. Nå kan Novartis og Sykehusinnkjøp sluttføre prisforhandlingene.'
Konkret betyr dagens vedtak i Beslutningsforum at sykehusene og produsenten Novartis vil dele den finansielle risikoen basert på resultatet av behandlingen - det vil si oppnådd helsegevinst med Zolgensma. Hva som defineres som oppnådd helsegevinst vil avgjøres av avtalen. Forhold som behandlingsrespons og varighet av respons vil typisk være resultater man kommer til å vektlegge i en slik avtale.
En slik prismodell har aldri før vært brukt i innkjøp av legemidler i Norge. Bryne ønsker ikke å gi ytterligere detaljer på hva prismodellen innebærer.
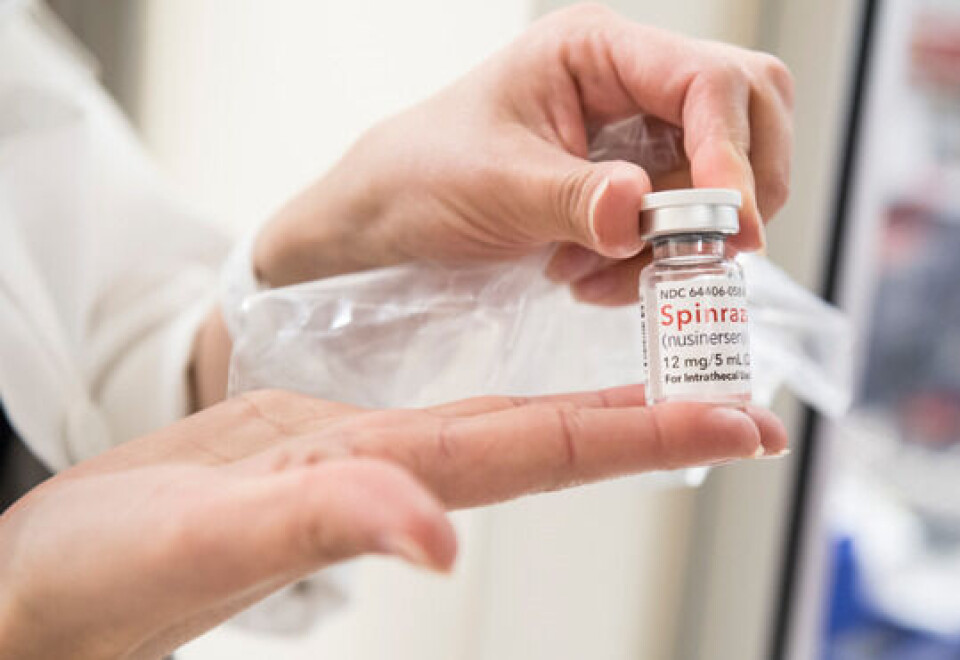
Spinal muskelatrofi er en alvorlig, arvelig sykdom som fører til tap av nerveceller i musklene, som igjen medfører muskelsvekkelse. Hvert år blir det født cirka 7 barn med SMA i Norge. Sykdommen kan ha ulik alvorlighetsgrad, og den mest alvorlige formen har vært en av de vanligste årsakene til tidlig barnedød i Norge. De mindre alvorlige formene gir tap av muskelkraft, og barna vil ikke kunne gå uten hjelp. I februar 2018 godkjente Beslutningsforum å ta i bruk Spinraza (nusinersen) ved SMA på gitte vilkår som i praksis er tilfredsstilt hos de fleste barn med nydiagnostisert SMA.
Beslutningsforum og Sykehusinnkjøp - som forhandler pris med legemiddelfirmaene - har så langt kun vært villig til å inngå prisavtaler der legemiddelfirmaene gir prosentvise rabatter på legemidlenes listepris - som kalles apotekenes utsalgspris - forkortet AUP. Utfordringen er imidlertid at avanserte legemidler - behandling med gen-, celle- eller vevsterapi - har en så høy AUP at det er krevende å inngå prisavtaler som er bærekraftige og akseptable for begge parter. At beslutningsforum før innføringen av genterapien Luxturna så langt bare hadde innført ett annet avansert legemiddel, understreker utfordringen. Det var celleterapien/CAR-T behandlingen Kymriah til behandling av akutt lymfoblastisk leukemi (ALL) for barn og unge som Beslutningsforum sa ja til å innføre i desember 2018.
Med dagens vedtak kan Novartis og Sykehusinnkjøp sluttføre prisforhandlingene over det som blir kalt verdens dyreste legemiddel. Listeprisen på engangsbehandlingen er om lag 20 millioner kroner per pasient. Når forhandlingene er sluttført blir det opp til Beslutningsforum å vurdere avtalen er god nok for sykehusene til at Zolgensma kan tilbys norske pasienter.
- Beslutningsforum ber leverandøren redusere prisen på produktet vesentlig slik at det er mulig å oppfylle prioriteringskriteriene. Dette er en forutsetning for at arbeidet med alternativ avtale kan fortsette. Forutsetningene i avtalen og eventuelle vilkår skal være forelagt den nasjonale faggruppen for spinal muskelatrofi før saken legges fram for ny vurdering i Beslutningsforum for nye metoder. Dette skal sikre at effektmålene er faglig relevante og praktisk gjennomførbare, sier Bryne.
Dansk modell
Etter det HealthTalk erfarer har Novartis og Sykehusinnkjøp blant annet sett til Danmark. Der vedtok Medicinrådet - som tilsvarer Beslutningsforum - den 27. april i fjor å innføre genetarapien Luxturna som standardbehanding i Danmark basert på en prismodell der helseregionene betaler for legemidlet i avdrag i stedet for hele beløpet på en gang - og at de kun betaler for behandlinger som har en vedvarende effekt. Pasientene skal nemlig til kontroll på fastsatte tidspunkter, og hvis det viser seg at legemidlet ikke har den ønskede effekt så skal de etterfølgende avdragene ikke betales.
Kan også gjelde andre avanserte legemidler
Dagens vedtak betyr at det åpner seg for muligheter for at også andre avanserte legemidler kan få tilsvarende avtaler med Sykehusinnkjøp. Det er i så fall gode nyheter for Bristol Myers Squibb som snart kommer til få markedsføringstillatelse for sin CAR-T celleterapi ide-cel. Noe senere er det forventet at også Janssen med sin CAR-T celleterapi cilta-cel får markedsføringstillatelse. Inger Cathrine Bryne forteller at dette vil Beslutningsforum tar stilling til fra sak til sak.
Nylig har det europeiske legemiddelbyrået EMA anbefalt at EU-kommisjonen gir markedsføringstillatelse til tre genterapier og som vil komme opp til vedtak i Beslutningsforum:
- Skysona (elivaldogen autotemcel) som blir den første godkjente genterapien mot den alvorlige nevrologiske sykdommen cerebral adrenoleukodystrofi.
- Bylvay (odevixibat) som blir den første medisinske behandlingen av sykdommen Progressiv familiær intrahepatisk kolestase (PFIC)
- Imcivree (setmelanotid) for pasienter fra seks år med fedme som skyldes genetisk feil på ett av tre ulike proteiner, POMC, PCSK1 og LEPR.
Usikkerhet om langtidseffekten
Engangsbehandlingen Zolgensma har en AUP på om lag 20 millioner kroner per pasient og beskrives som verdens dyreste legemiddel.
Sykehusinnkjøp og Novartis Gene Therapies har i lengre tid forhandlet om ulike prismodeller som vil gjøre at produsenten og Sykehusinnkjøp kan bli enige om en avtale som kan legges frem for Beslutningsforum. Nå kan partene gå tilbake til forhandlingsbordet og ferdigstille forhandlingene.
- Novartis Gene Therapies har over en lengre periode hatt et konstruktivt samarbeid med myndighetene for å finne en løsning som er bærekraftig og akseptabel for alle parter. Vi ser at disse nye genterapiene har utfordret det etablerte systemet i Nye metoder. Eksempelvis ved at det er usikkerhet rundt langtidseffekten. Pasienten man har fulgt lengst fikk behandling med Zolgensma for over seks år siden. Alle våre studiedata viser at effekten av behandlingen fortsatt vedvarer. Likevel er det forståelig at myndighetene ønsker god dokumentasjon for langtidseffektene, forteller Sissel Rodahl. Hun er daglig leder i Novartis Gene Therapies for området European Mid-Sized Countries.
- Derfor har vi i forhandlingene med Sykehusinnkjøp diskutert en avtalemodell som inneholder elementer av risikodeling, for eksempel basert på resultat av behandlingen. Utover dette kan vi ikke kommentere nærmere den konkrete modellen eller prisene som er foreslått, sier hun.
Sa ja til ny brystkreftmedisin
I dag vedtok Beslutningsforum også å innføre PARP-hemmeren Talzenna (talazoparib) til behandling av voksne pasienter med BRCA1/2-mutasjoner som har HER2-negativ lokalavansert eller metastatisk brystkreft. I fjor sa Beslutningsforum nei til å innføre legemidlet, og årsaken til dagens positive vedtak skyldes av produsenten Pfizer har redusert prisen opplyser fagdirektør i Helse-Vest Baard-Christian Schem.
Beslutningsforum sa også ja til å innføre Venclyxto (venetoklaks) til behandling av voksne pasienter med tidligere ubehandlet kronisk lymfatisk leukemi (KLL).