Legemidler og biotek
En kur for arvelige blodsykdommer: Lovende behandlingsresultater med CRISPR genredigering
Ti pasienter med alvorlige varianter av blodsykdommene sigdecelleanemi eller talassemi som ble behandlet med TX001, en CRISPR-basert terapi er fri for symptomer på sykdommene og trenger ikke lenger blodtransfusjoner. De er dermed funksjonelt kurert selv om oppfølgingstiden i studiene fremdeles er relativt kort. Dette markerer en sentral milepæl for anvendelsen av den banebrytende genredigeringsteknologien CRISPR.
Resultatene som ble presentert på konferansen American Society of Hematology på lørdag, kommer fra to banebrytende tidligfasestudier av en behandling som kalles CTX001 som er utviklet av bioteknologiselskapene CRISPR Therapeutics og Vertex i partnerskap.
Studiene ble samtidig publisert i The New England Journal of Medicine.
Syv pasienter med talassemi
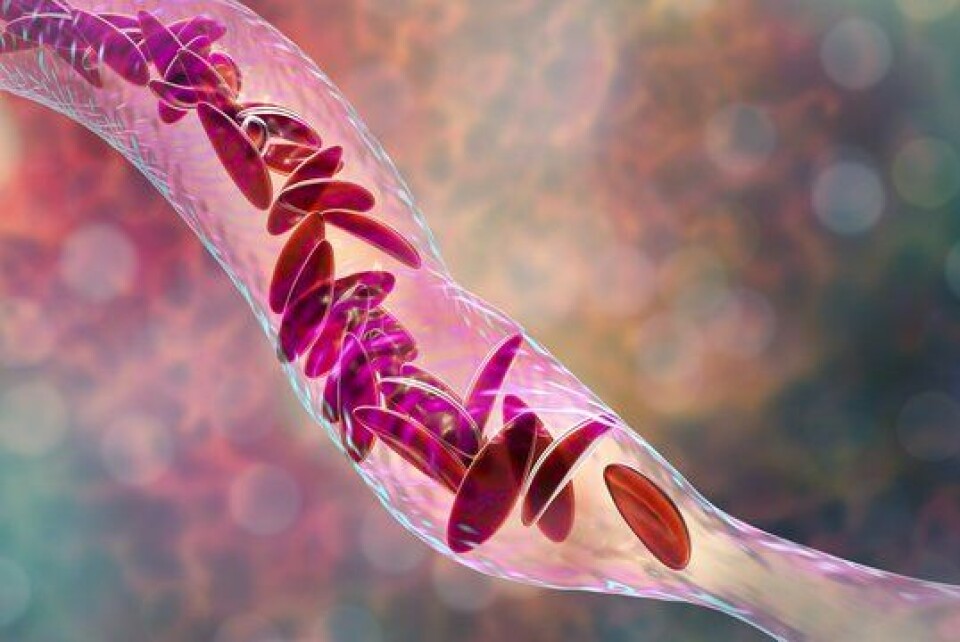
Talassemi skyldes en skade i et av genene som lager hemoglobin. Hemoglobin er det stoffet som sørger for oksygentransporten i blodet, og når hemoglobinnivået er lavt, får personen anemi. For de fleste finnes ingen behandling som kan helbrede talassemi. Ved alvorlig talassemi er det derfor helt nødvendig med hyppige, regelmessige blodoverføringer. Behandlingen må vare livet ut.
I en studie med syv talassemipasienter trengte ingen av dem blodoverføringer i minst tre måneder etter at de ble behandlet med CTX001. En pasient har klart seg uten blodoverføring så lenge som 18 måneder etter CRISPR-behandlingen. Fire pasienter har klart seg i seks måneder og en pasient har oppnådd ett år med vedvarende effekt av behandlingen.
Før disse pasientene fikk CTX001, gjennomgikk de median 15 blodoverføringer per år.
Tre pasienter med sigdecelleanemi
I den andre studien ble tre pasienter med sigdecelleanemi behandlet med CTX001.
Sigdecelleanemi er en medfødt sykdom som forårsaker anemi, det vil si lav blodprosent. Årsaken til sykdommen er en skade i et av genene som lager hemoglobin. I ungdomsårene og voksen alder er akutte episoder på grunn av tette blodårer vanlig. Dette kan gi sterke smerter, særlig i knokler, men også i indre organer.
Pasientene som ble behandlet med CTX001 har ikke opplevd noen forekomster av “uutholdelige smerteepisoder” i minst tre måneder og opp til 17 måneder. Før de ble med i studien hadde pasientene en median på syv uutholdelige smerteepisoder per år.
Tror det kan være en engangsbehandling
Alle 10 pasienter produserer nå "normale til nesten normale" nivåer av det oksygenbærende proteinet hemoglobin, som enten mangler eller er endret hos personer med alvorlig talassemi eller sigdecelleanemi.
Så langt har effekten av behandlingen ikke avtatt sier selskapene, og resultatene var uavhengig av hver pasients sykdoms alvorlighetsgrad eller underliggende genetiske egenskaper.
- Vi har store forhåpninger til at dette kan være en engangsbehandling som er kurativ for livet, sa CRISPR Therapeutics-sjef Sam Kulkarni i et intervju etter studiene ble presentert.
For mange av pasientene i studiene er resultatene fremdeles tidlige, med oppfølging i bare tre til seks måneder. Hvorvidt de positive effektene vil avta for noen, er usikkert.
Svært dyre legemidler
Det som imidlertid er sikkert, er at nå kommer legemidler basert på celle- og genterapi innen flere diagnoser - blant annet kreft og hemofili - som kan kurere alvorlige kroniske sykdommer med bare én behandling. Dermed kan pasientene slippe livslang medisinering og legebesøk.
Genterapien Zolegensma fra Novartis Gene Therapies - har en prislapp på rett under 20 millioner kroner per pasient og er allerede godkjent i USA. Det europeiske legemiddelverket (EMA) sitt ekspertpanel for godkjenning av legemidler (CHMP) ga i mai i år en betinget godkjenning av Zolgensma for visse pasienter er under godkjenningsprosedyre i Europa. Legemidlet er en engangsbehandling av spedbarn med spinal muskelatrofi (SMA).
Korte studier med få pasienter
Oppfølgingen i studier av disse nye legemidlene er ofte korte, i blant bare et par år og antall pasienter i studiene er ofte få. Spørsmålet som legemiddelmyndighetene stiller seg er om de er sikre og helbredende, eller kommer sykdommen tilbake?
Prislappen er satt med en forutsetning at legemidlet er kurerende, men det er ingen som med sikkerhet kan si at det vil ha effekt livet ut. Det gjør at både industrien og myndighetene nå stiller seg spørsmålet om hvem som skal bære risikoen om legemidlene ikke holder det de lover - er det skattebetalerne eller selskapene?
I Norge har Bestillerforum sagt nei til å starte en hurtig metodevurdering av Zolgensma. Begrunnelsen er at Novartis ikke har levert tilstrekkelig dokumentasjon til at Statens legemiddelverk kan utarbeide en kostnad-nytte-vurdering. Dette betyr at en innføring av denne genterapibehandlingen er utsatt på ubestemt tid.
Overvåkes for bivirkninger
Studiedeltakere blir overvåket for eventuelle bivirkninger. CRISPR og Vertex rapporterte om en alvorlig bivirkning som kan være relatert til CTX001; nemlig ett tilfelle av en potensielt livstruende immunreaksjon.