Relatert innhold
Avastin forbedret effekten av kjemo
Resultater fra en kinesisk fase 3-studie viser at tillegget av bevacizumab ga betydelig lengre sykdomskontroll i hjernen og høyere responsrater sammenlignet med kjemoterapi alene.
Median intracerebral progresjonsfri overlevelse ble nesten doblet med bevacizumab (11 vs. 6 mnd). Pasientene hadde også høyere respons i både hjernen (70 % vs. 32 %) og systemisk (58 % vs. 27 %), og flere oppnådde remisjon av hjerneødem (89 % vs. 35 %). Median totaloverlevelse var numerisk lengre (28,1 vs. 18,5 mnd), men forskjellen var ikke statistisk signifikant. Sikkerhetsprofilen var akseptabel.
ADC bremset hjernemetastaser
En analyse fra TROPION-Lung01 viser at pasienter med hjernemetastaser hadde bedre intracerebral respons og lengre sykdomskontroll med datopotamab deruxtecan (Dato-DXd) enn med docetaksel.
Blant pasientene med ubehandlede og målbare metastaser i hjernen oppnådde 37,5 % respons på Dato-DXd, inkludert én komplett respons, mens ingen i docetaksel-gruppen responderte. Median tid til intracerebral respons var 1,5 måneder.
Median intracranial PFS var 5,1 måneder med Dato-DXd mot 4,4 måneder med docetaksel (HR 0,65). Gevinsten var tydeligst hos pasienter med ubehandlet eller progrediert sykdom etter strålebehandling (5,0 vs. 3,0 mnd; HR 0,48).
Resultatene samsvarer med funnene fra TROPION-Lung05 og styrker evidensen for Dato-DXd ved NSCLC med hjernemetastaser, skriver forskerne.
Cemiplimab gir lang overlevelse
Femårsdata fra fase 3-studien EMPOWER-Lung 3 viser at førstelinjebehandling med cemiplimab pluss kjemoterapi gir en betydelig og varig forbedring i totaloverlevelse sammenlignet med kjemoterapi alene – både ved plateepitel- og ikke-plateepitel NSCLC.
Den dobbeltblindede, placebokontrollerte fase 3-studien inkluderte 466 pasienter med avansert, tidligere ubehandlet ikke-småcellet lungekreft (NSCLC) uten EGFR-, ALK- eller ROS1-aberrasjoner. Pasientene ble randomisert 2:1 til cemiplimab kombinert med kjemoterapi eller kjemoterapi alene.
Etter en median oppfølging på over fem år var median totaloverlevelse 21,1 måneder for kombinasjonsbehandlingen mot 12,9 måneder for kjemoterapi alene (HR 0,66; p=0,0002). Femårs overlevelse var mer enn doblet: 19,4 % vs. 8,8 %.
Fordelen ble sett på tvers av histologier.
- Plateepitel NSCLC: Median OS 22,3 vs. 13,8 mnd (HR 0,68).
- Ikke-plateepitel NSCLC: Median OS 19,4 vs. 12,4 mnd (HR 0,62).
Blant pasienter med PD-L1 ≥1 % var median OS hele 24 måneder med kombinasjonsbehandlingen mot 12,1 måneder med kjemoterapi (HR 0,54).
Kombinasjonsarmen hadde en objektiv responsrate på 44 % mot 22 % i kontrollarmen, og 6,4 % av pasientene oppnådde komplett respons (CR) mot ingen i kontrollgruppen. Median responsvarighet var 16,4 måneder mot 7,3 måneder.
Av de 312 pasientene som fikk cemiplimab pluss kjemoterapi, fullførte 21 % hele to års behandling. Denne gruppen hadde en imponerende femårs overlevelse på 56 %.
Grad ≥3 behandlingsrelaterte bivirkninger forekom hos 49 % av pasientene som fikk kombinasjonsbehandling, sammenlignet med 33 % i kontrollarmen. Sikkerhetsprofilen var i tråd med tidligere rapporterte data.
– Disse femårsdataene bekrefter at cemiplimab kombinert med kjemoterapi gir varig overlevelsesgevinst og bør regnes som en viktig førstelinjestandard for pasienter med avansert NSCLC, sier forskerne bak studien.
Osimertinib bedret sykdomskontroll
Interimdata fra COMPEL-studien viser at pasienter med EGFR-mutert NSCLC som fortsatte med osimertinib kombinert med platinabasert kjemoterapi hadde lengre progresjonsfri overlevelse enn dem som fikk kjemoterapi alene.
Den globale fase 3-studien ble avsluttet tidlig etter endringer i behandlingslandskapet, og inkluderte til slutt 98 pasienter som hadde progrediert på førstelinje osimertinib uten intrakraniell progresjon. Omtrent en tredjedel hadde hjernemetastaser ved inklusjon.
Median PFS var 8,4 måneder for kombinasjonsbehandlingen mot 4,4 måneder for kjemoterapi alene. Blant pasientene uten hjernemetastaser ved baseline hadde 87 % i kombinasjonsarmen PFS på 6 måneder, mot 63 % i kontrollarmen (HR 0,56). Median CNS-PFS var 15,9 vs. 8,6 måneder.

Giulia Pasello, MD, PhD Foto: WCLC Pasienter som fortsatte med osimertinib hadde også færre nye lesjoner totalt (18 % vs. 25 %) og færre nye hjernemetastaser (5 % vs. 13 %). Ved progresjon hadde 10 % i kombinasjonsarmen utviklet nye hjernelesjoner, mot 27 % i kontrollarmen.
Ettårs overlevelse var 67 % i kombinasjonsarmen og 47 % i kontrollarmen. Median totaloverlevelse var 15,9 vs. 9,8 måneder (HR 0,71), men dataene var umodne og ikke statistisk signifikante.
Bivirkningsprofilen var i tråd med det man kjenner fra kombinasjonen av osimertinib og platinabasert kjemoterapi, uten nye sikkerhetsfunn.
– Osimertinib kan fortsatt gi en beskyttende effekt i CNS etter progresjon, og disse funnene støtter videre utforskning av denne strategien, sa Dr. Giulia Pasello, University of Padova, som presenterte resultatene under WCLC 2025.
Bjørn Henning Grønberg: Nye overlevelsesdata
– Den største nyheten på årets verdenskongress for lungekreft i Barcelona var nok overlevelsesdataene fra FLAURA2-studien, sier Bjørn Henning Grønberg.
Han mener de nye resultatene viser en reell og meningsfull forlengelse av overlevelsen for pasienter med EGFR-mutert lungekreft.
Svulststørrelse avgjør effekten
I CURB-studien hadde pasienter med mindre målbare voksende svulster ved oligoprogresjon betydelig bedre progresjonsfri og total overlevelse etter stereotaktisk kroppsstrålebehandling (SBRT) enn pasienter med større tumorbyrde.
Forskerne fant at en samlet diameter ≤ 4 cm for voksende lesjoner ga en median overlevelse på over 60 måneder, mot kun 11 måneder hos dem med større lesjoner. Totalt antall svulster eller mønster for progresjon hadde ingen betydning. Levermetastaser var derimot assosiert med kortere levetid. Resultatene peker på at det er størrelsen på de aktive svulstene som er viktigst når man vurderer videre behandling.
Ny ADC ga rekordlang PFS
En ny bispesifikk antistoff-legemiddelkonjugat (ADC), iza-bren, har i to fase II-studier vist de lengste progresjonsfrie overlevelsestallene som hittil er rapportert for EGFR-mutert ikke-småcellet lungekreft (NSCLC).
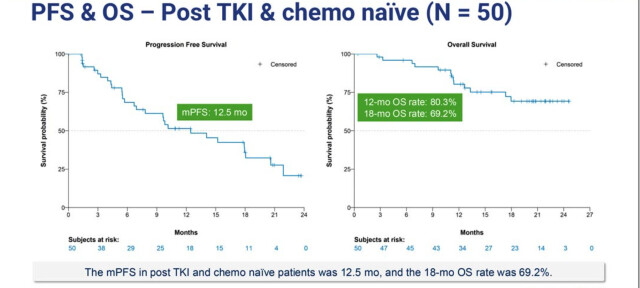
I monoterapi hos 171 tidligere behandlede pasienter med lokalt avansert eller metastatisk sykdom oppnådde en undergruppe på 50 pasienter som fikk 2,5 mg/kg dag 1 og dag 8 hver tredje uke en objektiv responsrate (ORR) på 66 % (bekreftet ORR 56 %), median PFS på 12,5 måneder og en median responsvarighet på 13,7 måneder. Nesten alle pasienter (94 %) hadde tumorkrymping, og 12-måneders OS-raten var 80,3 %, selv om median OS ikke var nådd ved datakutt. –Til min kunnskap er dette den lengste PFS som er rapportert for et ADC, sa studiens hovedutprøver Wenfeng Fang, MD, PhD.
Kilde; WCLC I kombinasjon med osimertinib som førstelinjebehandling viste iza-bren enda mer oppsiktsvekkende resultater. Blant 40 pasienter hadde 95 % bekreftet respons (38 pasienter), og alle fikk tumorkrymping med en median reduksjon på 56,7 %. Etter 12 måneder var PFS 92,1 % og OS 94,8 %. –Disse resultatene er bemerkelsesverdige og antyder at kombinasjonen kan bli et potensielt transformativt førstelinjealternativ for EGFR-mutert NSCLC, sa Fei Zhou, MD, PhD.
Sikkerhetsprofilen var konsistent med tidligere studier. Hyppigste bivirkninger var hematologiske, inkludert anemi, leukopeni, nøytropeni og trombocytopeni. Ikke-hematologiske bivirkninger omfattet kvalme, alopeci og stomatitt. Alvorlige hendelser grad 3–4 forekom, men ble håndtert med dosejusteringer eller støttende behandling. Det var ingen behandlingsrelaterte dødsfall.
Pågående fase III-studier i Kina undersøker nå iza-bren som monoterapi etter progresjon på tredjegenerasjons EGFR-TKI, samt som førstelinjebehandling i kombinasjon med osimertinib.
ADC viser lovende effekt i småcellet
En fase 1-studie med 80 pasienter viste at ABBV-706 ga klinisk meningsfulle responser i tidligere behandlede småcellete lungekreftpasienter, særlig i andrelinje og hos pasienter uten tidligere Top1i-behandling.
ABBV-706, et legemiddel som kombinerer et antistoff med en kraftig cellegift. Responsraten var over 60 % i utvalgte grupper, og varigheten av respons var lengre ved 1,8 mg/kg enn 2,5 mg/kg. Selv om alvorlige bivirkninger som anemi og neutropeni forekom, ble sikkerheten vurdert som håndterbar. Den anbefalte dosen er nå satt til 1,8 mg/kg hver tredje uke.
Immunterapi-kombo skuffer
I NIVIPI-BRAIN-studien oppnådde pasienter med NSCLC og ubehandlede hjernemetastaser lavere intracranial progresjonsfri overlevelse enn ventet, selv om noen fikk gode responser.
Pasientene fikk en kombinasjon av nivolumab, ipilimumab og to kurer kjemoterapi. Intracranial progresjonsfri overlevelse var kortere enn systemisk, og kun rundt 40 % oppnådde sykdomskontroll i hjernen etter 5–6 måneder. Totalt levde pasientene i median 10,6 måneder. Nevrologiske bivirkninger forekom, men var som regel milde til moderate.
Forbedret progresjonsfri overlevelse
Fase 3-studien ACROSS 2 viser at pasienter med avansert EGFR-mutert NSCLC og samtidig tumorsuppressorgens-mutasjoner hadde lengre progresjonsfri overlevelse når aumolertinib ble kombinert med kjemoterapi.
Median PFS var 19,8 måneder med kombinasjon versus 16,5 måneder med monoterapi (HR 0,55; p=0,0205). Foreløpige data for totaloverlevelse er umodne. Sikkerhetsprofilen var håndterbar, og ingen nye bivirkningssignaler ble observert.
Studien peker på at kombinasjonsbehandling kan være et bedre førstelinjealternativ enn EGFR-TKI alene for denne høy-risiko pasientgruppen.
Tagrisso + kjemo ga lengre overlevelse
Den endelige analysen fra fase 3-studien FLAURA2 viser at kombinasjonen av osimertinib og kjemoterapi ga signifikant bedre totaloverlevelse (OS) enn osimertinib alene hos pasienter med avansert EGFR-mutert ikke-småcellet lungekreft (NSCLC). Resultatene ble presentert 7. september under Presidential Symposium på WCLC.
I analysen hadde pasientene som fikk kombinasjonsbehandlingen en median OS på 47,5 måneder – nesten fire år – sammenlignet med 37,6 måneder (ca. tre år) for dem som fikk osimertinib monoterapi. Med 57 % datamodenhet reduserte kombinasjonen risikoen for død med 23 % (HR 0,77; 95 % CI 0,61–0,96; p=0,0202).
Etter tre år levde 63,1 % av pasientene i kombinasjonsarmen, mot 50,9 % i monoterapiarmen. Etter fire år var tallene 49,1 % versus 40,8 %. Gevinsten var konsistent på tvers av alle forhåndsdefinerte undergrupper. Pasienter i kontrollarmen mottok etterfølgende behandling i tråd med dagens standard, inkludert kjemoterapi, noe som understreker robustheten i OS-resultatene.
–Formålet med behandling av lungekreft i et stadium hvor sykdommen har spredt seg, er å forlenge overlevelsen, samtidig som pasientens livskvalitet opprettholdes. De positive resultatene fra denne studien, som viser en statistisk signifikant økning i median totaloverlevelse, bekrefter at denne kombinasjonsbehandlingen bidrar til å oppnå begge disse behandlingsmålene. Studien støtter bruk av osimertinib, med eller uten tillegg av kjemoterapi, som standard førstelinjebehandling for pasienter med avansert EGFR-mutert lungekreft, sier David Planchard, onkolog ved Gustave Roussy Institute of Oncology i Villejuif, Frankrike, og hovedutprøver for studien.

– Studien støtter bruk av osimertinib, med eller uten tillegg av kjemoterapi, som standard førstelinjebehandling for pasienter med avansert EGFR-mutert lungekreft, sier David Planchard, som var hovedutprøver for studien. Foto: WCLC –De nyeste resultatene fra FLAURA2-studien setter en ny standard for overlevelse for disse pasientene. I løpet av det siste tiåret har osimertinib konsekvent levert markante overlevelsesfordeler og vist god tolererbarhet på tvers av alle stadier av ikke-småcellet lungekreft. Osimertinib har dermed befestet sin rolle som en helt sentral komponent i all behandling av EGFR-mutert lungekreft, sier Susan Galbraith, Executive Vice President, Oncology Haematology R&D i AstraZeneca.
Bivirkningsprofilen til kombinasjonen var håndterbar og i tråd med det som er kjent fra de enkelte legemidlene. Bivirkninger av grad 3 eller høyere forekom hos 70 % i kombinasjonsarmen, mot 34 % i monoterapiarmen, og var i hovedsak kjemoterapirelaterte. Andelen som måtte avslutte behandling på grunn av bivirkninger var lav i begge armer (12 % vs. 7 %).
Atezolizumab ga økt sykdomskontroll
En fransk fase 3-studie viser at immunterapien Tecentriq (atezolizumab) kombinert med kjemoterapi gir lengre sykdomskontroll hos pasienter over 70 år med avansert NSCLC. Likevel ble det ikke påvist en signifikant gevinst i totaloverlevelse.
Studien inkluderte over 500 eldre pasienter. Tillegget av atezolizumab ga lenger tid uten sykdomsprogresjon og flere og mer varige responser, men median totaloverlevelse økte ikke signifikant. Bivirkningene var hyppigere og mer alvorlige i kombinasjonsgruppen.
Kombinasjon med niraparib skuffet
Fase 3-studien ZEAL-1L viste at kombinasjonen av PARP-hemmeren niraparib (Zejula) og immunterapien pembrolizumab ikke forbedret progresjonsfri overlevelse sammenlignet med pembrolizumab alene hos pasienter med avansert NSCLC som hadde hatt respons på førstelinjebehandling.
Studien inkluderte over 660 pasienter med stadium IIIB/IIIC–IV NSCLC. Pasientene ble randomisert til niraparib pluss pembrolizumab eller placebo pluss pembrolizumab som vedlikeholdsbehandling etter kjemoterapi og pembrolizumab førstelinje. Ved data cut-off viste resultatene ingen forbedring i PFS eller OS med kombinasjonen, og bivirkningsprofilen var i tråd med kjente sikkerhetsdata.
Fysisk aktivitet reduserer dødelighet
En stor koreansk kohortstudie viser at både vedlikehold og økning av fysisk aktivitet etter en lungekreftdiagnose gir betydelig redusert dødsrisiko, mens inaktivitet er forbundet med dårligere overlevelse.
Forskerne fulgte mer enn 23 000 personer med lungekreft som hadde deltatt i et nasjonalt helsescreeningsprogram i Sør-Korea. Deltakerne rapporterte aktivitetsnivå både før og etter diagnosen, og ble fulgt i opptil 12 år.
Resultatene viste en tydelig dose–respons-sammenheng: jo mer fysisk aktivitet, desto lavere risiko for å dø både av lungekreft og andre årsaker. Pasienter som holdt seg aktive både før og etter diagnosen hadde den beste prognosen, med en reduksjon i total dødelighet på nesten 30 prosent sammenlignet med dem som forble inaktive. Derimot hadde de som sluttet å være aktive etter diagnosen like dårlig overlevelse som pasienter som aldri trente.
Studien fremhever viktigheten av å opprettholde eller øke fysisk aktivitet etter lungekreftdiagnose for å oppnå best mulig overlevelse.
Fem års overlevelsesgevinst
Den endelige femårsanalysen fra fase 3-studien CheckMate 816 bekrefter at neoadjuvant nivolumab kombinert med kjemoterapi gir varig overlevelsesgevinst sammenlignet med kjemoterapi alene ved operabel NSCLC.
Studien inkluderte pasienter med stadium IB–IIIA ikke-småcellet lungekreft uten EGFR- eller ALK-mutasjoner. Deltakerne ble randomisert til tre kurer med kjemoterapi, med eller uten nivolumab, før kirurgi.
Etter nær seks års oppfølging hadde pasientene som fikk kombinasjonsbehandling en femårs overlevelse på 74 prosent, mot 63 prosent i kjemoterapiarmen. Gevinsten var tydelig blant dem som gjennomgikk definitiv kirurgi, uavhengig av operasjonsmetode og reseksjonsomfang. Sikkerhetsprofilen var i tråd med tidligere funn, og bivirkningene var håndterbare.
Forskerne konkluderer med at regimet bør anses som en standard neoadjuvant behandling for pasienter med operabel NSCLC.
Tagrisso gir mindre spor av kreft
En ny analyse fra fase 3-studien NeoADAURA viser at neoadjuvant behandling med Tagrisso (osimertinib), med eller uten kjemoterapi, økte andelen pasienter som fikk eliminert målbare spor av kreft i blodet før operasjon. Dette var koblet til bedre patologisk respons.
Studien inkluderte pasienter med operabel ikke-småcellet lungekreft (stadium II–IIIB) og EGFR-mutasjon. Totalt 189 pasienter hadde blodprøver som ble analysert med en ultrafølsom MRD-test basert på sirkulerende tumor-DNA (ctDNA).
Ved oppstart var 71 prosent MRD-positive. Etter behandling viste analysen at osimertinib, både alene og kombinert med kjemoterapi, ga betydelig høyere MRD-clearance (83–84 %) enn placebo med kjemoterapi (58 %). Pasienter som ble MRD-negative før kirurgi hadde bedre sykdomsfri overlevelse og oftere stor patologisk respons i tumorvevet.
Forskerne mener funnene understøtter at MRD-analyse kan bli et nyttig verktøy for å følge effekten av neoadjuvant behandling, og at osimertinib kan styrke behandlingsresultatene i denne pasientgruppen.
Ny immunterapi ga god respons
En fase II-studie viser at en ny immunterapikombinasjon med antistoffet tiragolumab og atezolizumab, med eller uten kjemoterapi, kan gi flere pasienter god respons før kirurgi ved lungekreft i tidlig stadium.
SKYSCRAPER-05-studien inkluderte 50 pasienter med operabel ikke-småcellet lungekreft. Behandlingen ble gitt før og etter kirurgi, og nesten alle pasientene kunne gjennomgå operasjon som planlagt.
I gruppen som fikk kombinasjonen med kjemoterapi oppnådde over halvparten av pasientene en betydelig tilbakegang av kreftvevet (major pathological response), og nær 3 av 10 hadde komplett fravær av kreftceller i vevsprøvene etter operasjon. Effekten ble sett på tvers av ulike PD-L1-nivåer. Bivirkningene var håndterbare og i tråd med det som er kjent fra tilsvarende behandlinger.
Gener og luftkvalitet avslører
En stor nederlandsk studie viser at genetiske risikoscorer og eksponering for svevestøv (PM2.5) kan bidra til å identifisere personer med høyere risiko for lungekreft. Funnene kan styrke risikostratifiseringen i screeningprogrammer og redusere unødvendige oppfølginger.
Forskerne analyserte data fra over 18 000 deltakere i to nederlandske kohorter, inkludert screeningstudien NELSON. De undersøkte polygenetiske risikoscorer (PRS) basert på kjente genetiske varianter knyttet til lungekreft, samt luftforurensning på bostedsnivå.
Resultatene viste at både genetiske risikoscorer og eksponering for fine partikler (PM2.5) var assosiert med økt sannsynlighet for lungekreft og lungekreftdødelighet. I tillegg kunne risikoscorene bidra til å skille bedre mellom pasienter med reell kreftsykdom og de med usikre funn på CT, noe som kan gjøre screening mer treffsikker og kostnadseffektiv.
Radon kan påvirker lungekreft
En spansk multisenterstudie viser at radoneksponering, særlig i kombinasjon med røyking, henger sammen med høyere tetthet av immunceller og et mer betent tumormikromiljø hos pasienter med ikke-småcellet lungekreft (NSCLC).
Forskerne inkluderte 750 pasienter med NSCLC fra 15 sykehus, og analyserte vevsprøver og eksponeringsdata fra 298 av dem. Radonnivåer i hjemmene ble målt, og røykevaner kartlagt.
Resultatene viste at radon, og særlig kombinasjonen av radon og røyking, var assosiert med økt innvekst av immunceller (tumor-infiltrerende lymfocytter) og en overvekt av «inflamed» tumormikromiljø. Dette kan tyde på at radon har en immunmodulerende effekt ved lungekreft. Forskerne mener videre studier er nødvendig for å forstå de kliniske konsekvensene.
Velkommen til vår livedekning av WCLC
Fra fredag 5. september dekker vi verdenskongressen for lungekreft WCLC, som går i Barcelona.
Vi lanserer et helt nytt livestudio for å dekke kongressen. WCLC er verdens største kongress innen lungekreft - og vi holder deg oppdatert!
I livestudioet får du:
- Korte nyhetsoppdateringer fra kongressen
- Videointervjuer med ledende helsepersonell
- Artikler om de mest spennende studiene som presenteres