Godkjenning av kreftlegemiddel ble tre år forsinket
– Allerede i 2019 var det åpenbart at en stor andel av lymfekreftpasientene som deltok i studiene var blitt helbredet av CAR-T behandlingen, men tvilen fikk for stor plass i Legemiddelverkets metodevurdering. Det sier overlege Alexander Fosså på Radiumhospitalet.
Han var en av tre medisinske fageksperter som Legemiddelverket brukte i metodevurderingen av den avanserte og kostbare celleterapien for behandling av sjeldne blodkreftsykdommen diffust storcellet B-cellelymfom (DLBCL). De to andre medisinske fagekspertene var overlegene Unn-Merete Fagerli på St.Olavs hospital og Bjørn Østenstad på Oslo universitetssykehus.
I et oppsiktsvekkende notat som er publisert på nyemetoder.no, er de tre toneangivende legene kritiske til at Legemiddelverket valgte å ikke lytte til deres faglige råd under metodevurderingen. Det skulle derfor gå tre år før Beslutningsforum i oktober i år innførte CAR-T legemidlet Yescarta til pasienter med den sjeldne blodkreftsykdommen. Da hadde legemidlet allerede vært i bruk i Finland og Sverige i to år. Beslutningsforum hadde avvist å innføre behandlingen to ganger tidligere – i september 2019 og i april 2021.
Et sted mellom 10 og 20 lymfekreftpasienter er aktuelle for behandling med Yescarta hver år i Norge.
Potensiale til å kurere
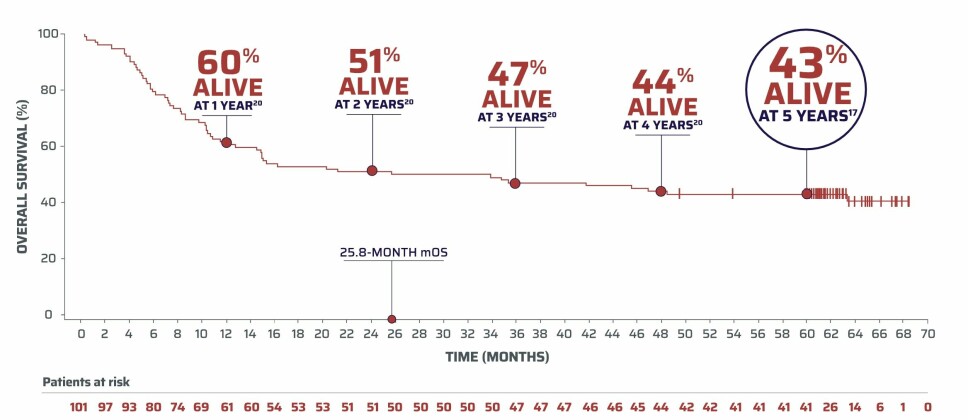
I notatet skriver de tre fagekspertene at de under metodevurderingen som ble utført i 2019 - to år etter at 111 pasienter hadde fått Yescarta i Zuma 1-studien - var trygge på at de kliniske dataene viste at behandlingen hadde potensiale til å kurere en stor andel av pasientene i det som kalles sene behandlingslinjer. Det betyr at pasientene som deltok i studien hadde fått flere andre behandlinger, men at kreften likevel var kommet tilbake.

Slik standardbehandling omfatter kjemoterapi, ofte i kombinasjon med antistoffet rituksimab. Stråleterapi kan være aktuelt, og pasienter kan også være kandidater for autolog stamcelletransplantasjon som er transplantasjon av bloddannende stamceller fra beinmarg.
– I sene behandlingsliner er det ytterst få av pasientene som blir kurert med kjemoterapi, og CAR-T er den siste behandlingen vi kan tilby pasientene. Behandling med Yescarta kan kurere om lag 40 prosent av pasientene i sene behandlingslinjer. De oppdaterte kliniske dataene som nå er publisert, viser at pasientene som ikke lenger hadde tegn til kreft to år etter behandlingen, nesten uten unntak også var kreftfrie etter fem år. Man kan si at disse pasientene etter to år nådde et platå som er ensbetydende med helbredelse, sier Fosså.
– Som fageksperter blir vi brukt til å belyse og gi premisser til modellene som biostatistikerne i Legemiddelverket bruker. Dessverre synes vi at metodene deres bommer litt på målet – de er rett og slett for overpresise og lykkes ikke i å beskrive en virkelig verden som er veldig usikker, sier Fosså.
Han mener at ekspertenes synspunkter ikke i tilstrekkelig grad ble hensyntatt i metodevurderingene.
– Legemiddelverket var for skeptiske til de oppsiktsvekkende behandlingsresultatene. Dermed tok det flere år å få innført en behandling som vi allerede i 2019 mente kunne ha en kurativ effekt for en del av pasientene. Effektdataene framstod for oss fageksperter allerede i 2019 som så gode og lovende at Beslutningsforum burde ha godkjent behandlingen allerede for tre år siden, sier Fosså.
– La tvilen komme behandlingen til gode
– Hvorfor går dere ut og forteller dette nå?
– Det kommer garantert flere slike betydelige medisinske fremskritt som Yescarta i tiden fremover. Vi håper at Legemiddelverket og Nye metoder kan ta lærdom av denne prosessen.
– Som ved andre vurderinger ga vi fageksperter våre råd skriftlig og muntlig i møter med Legemiddelverkets saksbehandlere, men våre råd har aldri før nå blitt lagt ved i saksdokumentene. Vi følte at tiden var moden for dette nå. Da vi ba om dette ble gjort, møtte vi ingen motforestillinger fra Nye metoder, sier Fosså.
Han forteller at en lærdom som kan trekkes er at når det råder usikkerhet om svært lovende effekter, bør Beslutningsforum la “tvilen komme behandlingen til gode”. – Å finne løsninger for midlertidige eller betingede godkjenninger er et åpenbart svar som gir mulighet til å trekke tilbake godkjenningen dersom data fra sanntidsbruk i Norge etter noen år skulle vise at behandlingsffekten ikke er så god som man initielt trodde, sier Fosså.
Bruker høy pris som syndebukk
CAR-T er ikke bare en effektiv, men også en svært kostbar behandling. Listeprisen (maksimal AUP) på Yescarta er rett i underkant av fire millioner kroner for en engangsbehandling (3 984 723 kr.), som ifølge Legemiddelverket ville gitt en merkostnad på 1,04 millioner kroner per vunnet kvalitetsjusterte leveår. Produsenten Gillead har gitt en rabatt, men denne er hemmelig.
Fosså mener det er viktig at Nye metoder ikke bruker usikkerhet rundt effektdata som en “syndebukk” når de i realiteten mener at prisen er for høy.
– Dersom det er skepsis til de kliniske resultatene, må dét komme tydelig frem i metodevurderingene. Når skepsisen først og fremst knytter seg til en høy legemiddelpris, må det flagges tydelig. Det er en ærlig sak. Det er viktig at det åpent kommuniseres at det blir for dyrt for helsevesenet, og ikke kamuflerer dette bak en kompleks matematisk beregning knyttet til usikkerheten om legemidlets effekt, sier Fosså. Han mener det er en gjennomgående svakhet i vurderingene til Nye metoder at man ikke evner å se annerledes på sjeldne kreftsykdommer.
Forstår utålmodigheten
Bjørn Egil Vikse er fagdirektør i Helse Vest og den mest sentrale medisinske rådgiveren til Beslutningsforum. Han har forståelse for utålmodigheten til klinikerne.
– Vi erkjenner og forstår at klinikerne har vært utålmodige i denne saken. Men vi må vurdere prisen opp mot nytteverdi. Nå har vi sagt ja til Yescarta, og jeg håper klinikerne er fornøyde med beslutningen denne gangen, sier Vikse.
Lederen i Beslutningsforum, Inger Cathrine Bryne, ønsker ikke å kommentere om metodevurderingene i for liten grad har tatt hensyn til de medisinske ekspertenes synspunkter.

– Det er ikke riktig av meg å kommentere metodevurderinger som er gjort helt tilbake i 2019. Men generelt vil jeg si at vi tar innspillene fra de kliniske ekspertene i metodevurderingene på største alvor, og vi jobber med forbedringsarbeidet på flere av Beslutningsforums områder, sier Inger Cathrine Bryne.
– Hva er din kommentar til at flere små pasientgrupper faller utenfor når metodevurderingene ikke tilpasses sjeldenhet?
– Fosså kan nok ha rett i at dette er et problem i noen saker, men generelt mener jeg at vi tar hensyn til sjeldenhet. Hadde vi ikke gjort det, ville vi ikke sagt ja til legemidler for sjeldne sykdommer, for vi godkjenner legemidler for pasientgrupper som er under ti pasienter årlig, sier Bryne.
Hun forteller at Nye metoder har opparbeidet seg en betydelig kunnskap om CAR-T celleterapi og at det i sommer ble inngått et avtaleverk for legemidler til gen- og celleterapier.
– Vi vet at det kommer en rekke gen- og celleterapier i framtiden. Da er det viktig at vi sørger for at prosessene kan gå raskest mulig. Målet med avtaleverket er å bidra til at pasienter får raskere tilgang til behandling, sier Bryne.